Урок 39/8. Обобщение знаний по теме «Изменения, происходящие с веществами»
Цель: обобщить и систематизировать знания
учащихся, полученные при изучении
темы.
Ход урока
I. Проверка домашнего задания.
Проверка
задач (стр.104, задания 3, 5).
II.
Зачет-конкурс.
Каждый
ряд выбирает капитана, класс делится. таким образом, на 3 команды.
1. Физические и химические явления.
Каждый
ряд получает листок бумаги, на котором поочередно пишут примеры химических
явлений. Нельзя повторять примеры предшествующие. В итоге получается большой
список химических явлений.
Дополнительный
вопрос. Приведите
признаки химических реакций.
2. Конкурс капитанов.
«Уравнять»
уравнения реакций.
1) Н2 + О2 ® Н2О 1)
Са + О2
® СаО
2) Al + HCl ® AlCl3 + H2 2)
Na + Н2О
® NaОН + H2
3) Мg(ОН)2 + HC ® МgСl2 + Н2О 3)
Аl(ОН)3
+ H2SO4 ® Al2(SO4)3 + Н2О
1)
К + О2
® К2О
2)
Са + Н3РО4 ® Са3(РО4)2 + Н2
3)
Са + НСl ® СаСl2 + Н2
4)
Р2О5 + Н2О ® Н3РО4
Капитаны
начинают с «верхних этажей», то капитан, который заканчивает первым,
расставляет коэффициенты в последнем уравнении.
3. «Аукцион знаний».
Учитель
задает вопросы, учащиеся отвечают на них, дополняют ответы:
Какие явления называются физическими?
Какие
явления называются химическими?
Приведите
примеры физических явлений.
Приведите
примеры химических явлений.
Каковы
признаки химических реакций?
Какие
условия необходимы для проведения химической реакции?
Когда
и кем был открыт закон сохранения массы веществ?
Приведите
формулировку этого закона.
Какие
типы химических реакций вы знаете?
Эта красавица всем вам знакома,
С ней вы
встречаетесь в школе и дома,
Бесцветна,
чиста почти,
Но ток
электрический включи -
И
разлагается она
На два
каких-то вещества.
(Н2О, вода)
Запишите
уравнение реакции разложения воды.
При каких условиях реакции обмена идут до
конца?
Я известна с давних пор и имею спрос,
Опусти
меня в раствор,
В медный
купорос.
Изменить
хочу я соль,
Ну-ка,
выйди, соизволь!
Удивительный
момент: стал другим раствор,
Вытесняю
элемент, не вступая в спор,
На меня
взгляни, ответь:
Начинаю
я ржаветь?
О
какой реакции идет речь? Запишите уравнение реакции.
4. Решение задачи «Кто быстрее?».
Найдите
ошибку!
Ученик
составил следующую задачу: «Железные опилки массой
Решение:
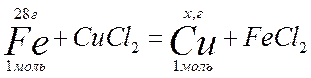
Составляем
пропорцию: 28/1 = х/1 х =
Ответ:
III. Подведение итогов урока.
IV. Домашнее задание:
1.
Решите задачу:
Кислородная
подушка вместимостью
2. Составьте задачу, обратную задаче
5, но со своими числами. Запишите ее текст,
решите наиболее рациональным способом.
Будь-те первым, поделитесь мнением с остальными.
